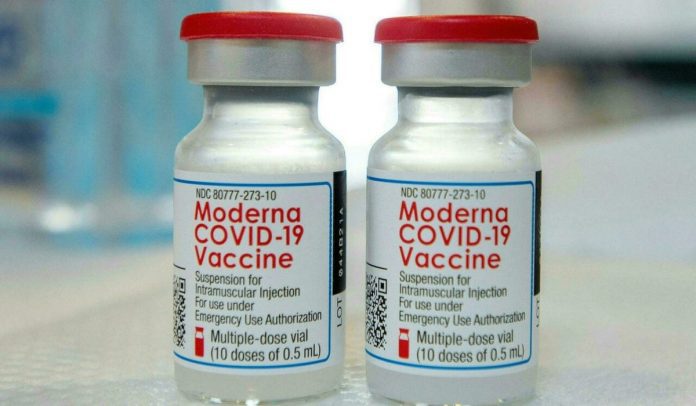
El Comité Científico de la Administración de Drogas y Medicamentos (FDA, por sus siglas en inglés) de Estados Unidos se reúne esta semana para definir si avala, o no, las dosis de refuerzo de las vacunas contra el Covid-19 desarrolladas por Moderna y Johnson and Johnson.
Los asesores en salud de la entidad dieron su aval al uso de una tercera dosis del fármaco de Moderna, inmunización que, en un principio, se había planteado solo para dos dosis, cada una de 100 microgramos. La tercera inyección sería de 50 microgramos, según adelantó la agencia AP.
No obstante, aún no se ha ratificado la decisión final de la FDA en relación con dicha autorización, pues el siguiente paso es que la entidad evalúe los apuntes de su Comité Científico para oficializar la determinación. (Ver más de Internacional).
Hasta ahora, la única vacuna contra el Covid-19 que cuenta con la aprobación del uso de emergencia de una dosis de refuerzo es la desarrollada por Pfizer/BioNTech, que utiliza el mismo sistema de la inoculación de Moderna: ARN mensajero (ARNm).
Recomendado: Científicos de la FDA desestiman refuerzo de vacuna Covid-19 de Moderna
Más de 69 millones de estadounidenses han recibido las dos dosis de la vacuna contra el Covid-19 de Moderna, de acuerdo con los Centros de Control de Enfermedades (CDC).
La autorización de la inyección de refuerzo aplicaría solo para las personas que hacen parte de la población en riesgo, es decir, que son mayores de 65 años o que presentan comorbilidades, lo que les hace más proclive a sufrir una infección grave.
La farmacéutica asegura que una dosis de refuerzo de su vacuna contra el Covid-19 trae “beneficios potenciales”, aumentando la barrera de protección ante el coronavirus.
Alrededor de 188,3 millones de personas en ese país ya están completamente vacunados y 9,3 millones han recibido la dosis de refuerzo del fármaco de Pfizer.
FDA prepara decisión sobre molnupiravir
El comité asesor de la FDA informó que se reunirá el próximo 30 de noviembre para discutir la solicitud de Merck y Ridgeback de una autorización de uso de emergencia para el molnupiravir, un medicamento antiviral en investigación que trata el Covid-19.
“Una discusión pública de estos datos ayudará a asegurar una comprensión clara de los datos científicos y la información que la FDA está evaluando para tomar una decisión sobre si autorizar este tratamiento para uso de emergencia ”, dijo Patrizia Cavazzoni, directora del Centro de Evaluación e Investigación de Medicamentos de la FDA.
—